钾离子通道
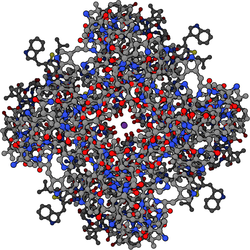
在细胞生物学的范畴,钾离子通道是最广泛分布的离子通道,且几乎存在大多数的生物中。[1] 它们形成横跨细胞膜而具钾离子选择性的孔洞,并且存在于大多数的细胞,控制了广泛的生物功能。[2][3]
种类
[编辑]钾离子通道主要有四种分类:
- 钙激活钾离子通道(Calcium-activated potassium channel):当钙离子或其它讯息分子出现时开启。
- 内向整流钾离子通道(Inwardly rectifying potassium channel):使正电荷(电流)由细胞外向细胞内流入较容易。
- 串联孔域钾离子通道(Tandem pore domain potassium channel):纵列孔洞钾离子通道:通道常开启或拥有基本的刺激,像是在神经细胞中的静止钾离子通道制造膜电位的负电性。
- 电压门控钾离子通道(Voltage-gated potassium channel):当膜内外电位产生改变时,此离子通道开合。
| 分类 | 次分类 | 功能 | 抑制物 | 活化物 |
|---|---|---|---|---|
| 钙激活 6T&1P | BK 通道, SK通道 | 抑制细胞内,因刺激而导致的钙增加。 | apamin, charybdotoxin | 1-EBIO, NS309, CyPPA |
| 内向整流 2T&1P | ROMK(Kir1.1) | 肾元中钾的回收及再利用 | 无选择性: Ba2+, Cs+ | 无 |
| GPCR 调控 (Kir3.x) | 调节多数GPCR中的抑制效应 | GPCR antagonists, ifenprodil[5] | GPCR agonists | |
| ATP敏感 (Kir6.x) | ATP浓度高足以刺激胰岛素分泌时关闭 | glibenclamide, tolbutamide | diazoxide, pinacidil | |
| 串联孔域 4T&2P | TWIK, TRAAK,TREK, TASK | 与静止电位有关 | 无 | halothane |
| 电压门控 6T&1P | hERG(Kv11.1), KvLQT1 (Kv7.1) | 动作电位再极化, 控制动作电位的频率(若受阻,产生节律障碍) | tetraethylammonium, 4-aminopyridine, dendrotoxins(在某些种类中) | 无 |
结构
[编辑]钾离子通道的结构由四条蛋白质次单位聚集而成,产生一个四折叠的对称复合物,其中心有一个离子引导孔洞的开合。四个相似的蛋白质次单位聚集产生一个heterotetrametic复合物 。钾离子通道的次单位在孔洞的顶端都绕成一个明显的孔洞结构,用来负责钾离子的选择性通透。
有超过80个哺乳动物基因用来制钾离子通道的次单位。细菌中,钾离子通道在分子结构中是最被为了解的离子通道。利用X光晶体绕射[6][7],我们了解到钾离子如何借由钾离子通道通过细胞膜,及为何钠离子无法通过。得知钠离子有较强电荷密度,因此周围被水分子围绕而变得较巨大。[8]2003年诺贝尔化学奖颁给在这个领域的先锋Rod MacKinnon。[9]
选择性滤嘴
[编辑]钾离子通道在钾离子通过选择性滤嘴时会移去水合层。选择性滤嘴是由每个次单位的p-loop上五个残基(TVGYG-原核物种)所形成,而每个次单元都含有连于过滤孔中心,电阴性的羰基氧原子,且在每个钾离子接合处周围形成反角柱状的水合层。碳氧基与过滤器钾离子接合处的距离与第一水合曾之水分子氧与水溶液中之钾离子距离相等。由于滤嘴与螺旋孔之间的强烈的相互作用,能预防通道萎陷为较小的钠离子通道大小,因此钠离之通行在电位能上是不利的。选择性滤嘴会朝向细胞外溶剂,让四个在甘氨酸残基上的碳氧基 (KcsA上的Gly79)裸露在细胞外。另一个朝细胞外的残基则是带负电的 Asp80 (KcsA)。这两个残基连同五个滤嘴的残基则形成连接胞外溶液与在蛋白中心的水充填腔之孔道。[10]
碳氧基为强的负电荷及正电荷的吸引基。过滤器能将钾离子安置于4个接合点,从细胞外结构开始标示起,标示为S1~ S4。另外,在腔道中一个离子能接合在称为SC接合处的地方,或者多个离子接在已被确定的接合点,称为S0或 Sext。许多不同的接合组态在这些接合点上是可能发生的。由于X光晶体绕射结构是许多分子之平均结构,因此不可能直接指出当下结合组态的结构。总括的说,有些缺点是两个邻近结合点都被离子结合而造成了静电排斥。在KcsA上之离子位移的机转已借由模拟技术被透彻的研究。一个完整的24=16态的自由能图(其特点为占有S1, S2, S3和S4之轨域)已经借由分子动力学之模拟计算出,结果指示此两个具有双轨域态之自由能,(S1, S3)及(S2, S4),在预测的离子传导机制里扮演重要的角色。在高浓度之钾离子的环境下形成之较好解析度的KcsA结构可发现Sext和S0这两个胞外状态。分子动力模拟包含了整个离子的所有路径,从腔室到通过四个滤嘴直到S0和Sext状态之自由能的计算。钾离子通道之选择性滤嘴的胺基酸序列是保守的,除了在真核的钾离子通道里的一个异亮氨酸残基常取代了原核之通道上的缬氨酸残基。氨基酸序列的选择性过滤器的钾离子通道是保守的,除了一个异亮氨酸残留在真核钾离子通道,常常是取代了缬氨酸残留在原核渠道。[10]
中央孔洞
[编辑]一个10埃宽的中央孔洞,位于跨膜通道的中心附近,由于通道壁斥水性的关系,对于要穿膜的离子来说此处的能量阻力最高。此充满水的腔室及孔螺旋之极性的C终端降低离子通过时的能量阻力。作者认为先前许多已通过的钾离子所形成的斥力增加离子的通过量。
阻断剂
[编辑]钾离子通道阻断剂,如4-Aminopyridine和3,4-Diaminopyridine,以被研究用以治疗如多发性硬化症等状况。[11]
一个由Andrew D. Goodman 等8人及由Acorda Therapeutics Inc.赞助的第三期临床试验显示fampridine(4-amonipyridine)有助于改善多发性硬化症病患的运动能力. 这个是一项随机分配,多中心,双盲,安慰剂对照的临床试验,一共收录了301位病患,以随机分配的方式229位病患使用fampridine(10mg bid), 79位使用安慰剂.这个临床试验已登录在ClinicalTrials.gov, 试验编号为NCT00127530,同时也在Lancet 2009 Feb, Vol.373, P732-39公开. 由于试验结果显示fampridine对多发性硬化症病患(虽然不是全部)相较于安慰剂组病患的运动能力有很大的改善,药物食品检验局部性(FDA)决定给予快速审核,于2009年10月22日将开会审议本药品[12].
参考文献
[编辑]- ^ Littleton JT, Ganetzky B. Ion channels and synaptic organization: analysis of the Drosophila genome. Neuron. 2000, 26 (1): 35–43. PMID 10798390. doi:10.1016/S0896-6273(00)81135-6.
- ^ Hille, Bertil. Chapter 5: Potassium Channels and Chloride Channels. Ion channels of excitable membranes. Sunderland, Mass: Sinauer. 2001: pages 131–168. ISBN 0-87893-321-2.
- ^ Jessell, Thomas M.; Kandel, Eric R.; Schwartz, James H. Chapter 6: Ion Channels. Principles of Neural Science 4th edition. New York: McGraw-Hill. 2000: pages 105–124. ISBN 0-8385-7701-6.
- ^ Rang, HP. Pharmacology. Edinburgh: Churchill Livingstone. 2003: page 60. ISBN 0-443-07145-4.
- ^ Kobayashi T, Washiyama K, Ikeda K. Inhibition of G protein-activated inwardly rectifying K+ channels by ifenprodil. Neuropsychopharmacology. 2006, 31 (3): 516–24. PMID 16123769. doi:10.1038/sj.npp.1300844.
- ^ Doyle DA, Morais Cabral J, Pfuetzner RA, Kuo A, Gulbis JM, Cohen SL, Chait BT, MacKinnon R. The structure of the potassium channel: molecular basis of K+ conduction and selectivity. Science. 1998, 280 (5360): 69–77. PMID 9525859. doi:10.1126/science.280.5360.69.
- ^ MacKinnon R, Cohen SL, Kuo A, Lee A, Chait BT. Structural conservation in prokaryotic and eukaryotic potassium channels. Science. 1998, 280 (5360): 106–9. PMID 9525854. doi:10.1126/science.280.5360.106.
- ^ Armstrong C. The vision of the pore. Science. 1998, 280 (5360): 56–7. PMID 9556453. doi:10.1126/science.280.5360.56.
- ^ The Nobel Prize in Chemistry 2003. The Nobel Foundation. [2007-11-16]. (原始内容存档于2012-10-26).
- ^ 10.0 10.1 Hellgren M, Sandberg L, Edholm O. A comparison between two prokaryotic potassium channels (KirBac1.1 and KcsA) in a molecular dynamics (MD) simulation study. Biophys. Chem. 2006, 120 (1): 1–9. PMID 16253415. doi:10.1016/j.bpc.2005.10.002.
- ^ Judge SI, Bever CT. Potassium channel blockers in multiple sclerosis: neuronal Kv channels and effects of symptomatic treatment. Pharmacol. Ther. July 2006, 111 (1): 224–59 [2008-12-09]. PMID 16472864. doi:10.1016/j.pharmthera.2005.10.006. (原始内容存档于2020-04-16).
- ^ Andrew D Goodman, Theodore R Brown, Lauren B Krupp, Randall T Schapiro, Steven R Schwid*, Ron Cohen, Lawrence N Marinucci, Andrew R Blight, etc, Sustained-release oral fampridine in multiple sclerosis: a randomised, double-blind, controlled trial. The Lancet, Vol.373 P.732-39, February 28, 2009
